Садржај
- Дефиниција
- Етилендиаминететрацетна киселина и потенциометријска метода
- Цомплекометриц Титратион
- Буретте Солутион
Научници се ослањају на директну титрацију како би пронашли количину неке супстанце у раствору са хемијским реакцијама. Ако се правилно изведе, овај поступак може врло прецизно приказати хемијске количине користећи специјализоване киселине и лабораторијско стаклено посуђе. Да би титрација радила правилно, последњи комплекс се мора формирати довољно брзо да га научници могу анализирати.
Дефиниција
Директна титрација је начин за квантитативно одређивање садржаја неке супстанце. Научници су можда свесни реактаната, али не знају количине реактанта. Директна титрација се понекад заснива на показатељима који одговарају на анализирани материјал, назван аналит. Други пут, методе се заснивају на употреби додатих јона метала, који су појединачни атоми или молекули одређене врсте метала.
Етилендиаминететрацетна киселина и потенциометријска метода
Техничари могу да врше титрацију применом етилендиаминететрацетне киселине са метал-јонским индикаторима. Ова метода не делује у свим ситуацијама, јер је реакција понекад толико спора да титрање постане нереално. Коришћени метални јони морају имати мању стабилност од аналита. Друга метода директне титрације је потенциометријска метода, која се користи за детекцију крајњих тачака са металним јонима који имају специфичне расположиве електроде. Крајња тачка је тачка у којој се процес титрације завршава.
Цомплекометриц Титратион
За комплексометријску титрацију, научници користе аминополикарбоксилне киселине да би идентификовали метале. Формирају се обојени комплекси, а научници користе податке прикупљене овом формацијом да би одредили количину аналита. Непосредна метода комплексометријске титрације укључује употребу метал-сонског раствора титрованог раствором сложених једињења. Комплексни раствори једињења садрже атоме или једињења која формирају комплексе са другим атомима или једињењима. Научници проналазе тачку еквиваленције из додатног показатеља. Тачка еквиваленције је када је додавани титрант стехиометријски једнак аналиту. Стехиометрија укључује уравнотежење хемијских реакција.
Буретте Солутион
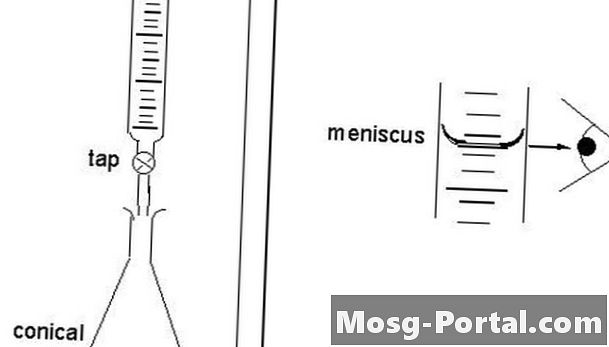
Директно титравање назива се "директно", јер научник директно приступа крајњој тачки. Титран улази у раствор капљицама из бирете тако да крајњи кап не надмаши крајњу тачку. Са директном титрацијом, научници третирају растворљиву супстанцу која се налази у раствору, а која се налази у посуди која се зове титрат. Стандардизовани раствор се назива титрант. Крајња тачка одређује се инструментално или визуелно уз помоћ индикатора. Научници додају титран у исправну биретту, вертикални и цилиндрични комад стакленог посуђа с прецизном славином која у одређеним количинама ослобађа мале количине течности. Научници пуне биретте до 30 до 100% капацитета.